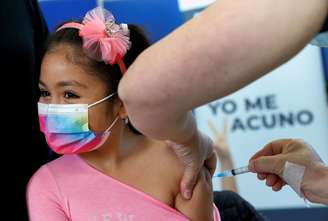
A Agência Nacional de Vigilância Sanitária (Anvisa) solicitou nesta quarta-feira, 22, mais informações e dados ao Instituto Butantan sobre a aplicação da vacina CoronaVac para crianças e adolescentes.
Segundo nota da autarquia, a exigência técnica foi enviada ao Butantan após a análise de documentos apresentados pelo instituto na quarta-feira da última semana, quando foi reapresentado o pedido de autorização da CoronaVac para a faixa etária de 3 a 17 anos.
"O pedido de exigência é comum nos processos de análise de vacinas. Este pedido não interrompe a análise pelos técnicos da Anvisa, que continuam trabalhando. Porém a exigência suspende a contagem do prazo de 30 dias que a Anvisa tem para avaliar o processo", afirmou a Agência.
Segundo a Anvisa, a solicitação de dados também tomou como base questionamentos de especialistas externos das áreas de imunologia e pediatria, que "indicaram lacunas importantes que ainda impedem afirmar de forma científica o grau de imunidade gerado nas crianças e adolescente".
Dentre os pontos levantados, os especialistas pedem mais dados sobre a chamada ponte imunológica que permite a extrapolação da eficácia da vacina em adultos para crianças. E também dados de segurança da CoronaVac separados por faixa etária das crianças dentro da idade que deve ser imunizada.
Em nota, o Butantan demonstrou surpresa com o pedido de informações da Anvisa e argumentou que entregou dossiês à Agência, além de ter enviado especialistas do laboratório para reunião com a agência. "É preciso que haja mais clareza por parte da Anvisa para que assuntos como a aprovação da vacina no contexto pandêmico que vivemos sejam tratados com a rapidez necessária", disse o instituto na nota.
Esse é o segundo pedido de autorização do uso da CoronaVac para crianças apresentado pelo Butantan. O primeiro, feito em agosto, também foi paralisado por falta de documentação suficiente.
O Butantan também ainda não entregou a documentação para pedido do registro definitivo da CoronaVac, apesar de ter sido a primeira a receber o registro emergencial. As vacinas Pfizer e Astrazeneca já receberam o registro definitivo.