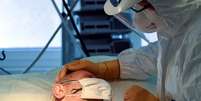
Em um esforço sem precedentes, a comunidade científica brasileira já se mobiliza na realização de pelo menos 76 estudos com seres humanos para entender o comportamento da covid-19 e buscar possíveis tratamentos.
O número está no mais recente balanço da Comissão Nacional de Ética em Pesquisa (Conep), órgão ligado ao Ministério da Saúde responsável por dar o aval para pesquisas que envolvam pessoas. Entre as investigações, a maioria (21) é de ensaios clínicos de possíveis tratamentos para a infecção.
Dez deles envolvem testes com cloroquina ou hidroxicloroquina, drogas que vêm sendo defendidas pelo presidente Jair Bolsonaro. As substâncias, mais conhecidas como antimaláricas, têm vários efeitos colaterais, principalmente relacionados a arritmias cardíacas. Até o momento se mostrou promissora em testes com poucas pessoas no mundo. Nenhum estudo em larga escala ainda foi capaz de mostrar sua eficácia.
O balanço, apresentado em relatório da Conep finalizado nesta terça-feira, 14, mostra ainda pesquisas com antibióticos, corticoides, plasma convalescente (de pessoas recuperadas) e até células-tronco mesenquimais. Mais de 8 mil pacientes participarão dos 21 estudos clínicos que buscam encontrar um tratamento para a covid-19. Os ensaios foram propostos por 17 instituições de pesquisa de cinco Estados. Entre elas estão centros renomados como a Faculdade de Medicina da USP, a Fundação Oswaldo Cruz (Fiocruz) e o Hospital Albert Einstein.
Dos dez estudos que envolvem remédios à base de cloroquina, três investigarão o uso isolado da substância, ou da sua variante menos tóxica, a hidroxicloroquina, e outros sete pesquisarão a eficácia da utilização do remédio associado ao antibiótico azitromicina.
Força-tarefa mundial
Um dos mais aguardados é o que está sendo coordenado pela Fiocruz para investigar a eficácia de quatro tratamentos contra a covid-19: a cloroquina e hidroxicloroquina, o remdesivir; uma combinação de dois medicamentos para o HIV, o lopinavir e o ritonavir; e a mesma combinação mais interferon-1A, um mensageiro do sistema imunológico que pode ajudar a paralisar o vírus.
O trabalho, que começou no fim de março, faz parte de um esforço mundial, coordenado pela Organização Mundial da Saúde, que está investigando essas quatro possibilidades de tratamento em vários países. No Brasil vão participar 18 hospitais de 12 Estados, com a expectativa de alcançar cerca de 1,2 mil pessoas.
Em uma modelagem dinâmica e adaptativa, o estudo vai permitir descartar drogas que eventualmente já se mostrarem inadequadas ao longo do estudo, assim como incluir outras. Mas, como ainda está muito no começo, não foi possível chegar a nenhuma conclusão desse tipo, de acordo com Estevão Portela Nunes, investigador principal do estudo no Instituto Nacional de Infectologia da Fiocruz.
Ainda não foi possível testar, por exemplo, o remdesivir, um medicamento usado contra o ebola que foi considerado promissor em alguns trabalhos, mas também carece de resultado em testes randomizados, quando os pacientes são escolhidos aleatoriamente e há um grupo controle. Esse é justamente o objetivo do projeto mundial. Os testes com essa droga não começaram porque ela ainda não chegou ao Brasil, o que se espera ocorrer até o fim do mês.
"A ideia é ter o máximo volume de pacientes em um tempo curto, com foco no desfecho clínico, se alguma modalidade de tratamento traz uma sobrevida ou alta. Estamos analisando essas drogas em comparação entre elas e com o cuidado padrão, que não envolve nenhuma medicação específica. A grande questão é ver se alguma vai se mostrar melhor que a outra. Se alguma for muito melhor, vamos ver isso rapidamente, mas ainda não temos isso", afirma Nunes.
Plasma e estudos observacionais
Outro trabalho que em breve deve ser iniciado vai usar plasma de pessoas que já tiveram contato com o coronavírus e se curaram. Foi montado um consórcio entre USP, USP de Ribeirão Preto, Unicamp e os hospitais Albert Einstein e Sírio Libanês para fazer um teste randomizado que vai checar a eficácia da aplicação do material em pacientes doentes. Serão testadas duas doses, uma de 200 ml e outra de 400 ml, na comparação com um grupo controle, que não vai receber o plasma.
O grupo já recebeu autorização da Conep para coletar o plasma e agora vai submeter o protocolo do teste clínico para iniciar os testes. Vanderson Rocha, diretor presidente da Fundação Pró-Sangue, do HC, afirma que já recebeu a inscrição de 90 possíveis doadores, sendo que 15 já foram capacitados. Pessoas que já foram testadas e confirmadas com a covid-19 e estão há mais de 14 dias sem sintomas podem doar o plasma para tratamento de pacientes com doença ativa.
Segundo Rocha, cada pessoa doa em média de 400 ml a 600 ml, o que pode fornecer material para até três testes. A expectativa é incluir de 90 a 120 pacientes no ensaio clínico.
Além dos 21 testes de possíveis tratamentos, a Conep deu aval ainda para outros 55 estudos observacionais relacionados à pandemia do coronavírus.
Entre as pesquisas propostas pelos cientistas estão estudos epidemiológicos, investigações sobre os impactos da quarentena e isolamento na saúde mental da população e de profissionais de saúde, detalhes sobre a manifestação da doença em crianças internadas com covid-19 e entre gestantes - dois grupos ainda pouco investigados.
Há trabalhos também sobre os fatores associados à adesão de medidas de prevenção contra o coronavírus, entre outros.
Estudo com cloroquina vira alvo nas redes e pesquisadores se defendem
Um estudo que vinha sendo conduzido com a cloroquina em Manaus - suspenso após se observar aumento de risco de complicações cardíacas - virou alvo em redes bolsonaristas, com os cientistas sendo chamados de irresponsáveis e acusados de usarem "cobaias humanas".
O CloroCovid-19, com 70 pesquisadores de instituições renomadas como Fiocruz, Universidade do Estado do Amazonas e da USP, havia sido autorizado pela Conep. Consistia em testar, em pacientes com suspeita de covid que apresentavam quadro de síndrome aguda respiratória grave (SRAG), duas dosagens de cloroquina: uma baixa e uma mais alta. A dose baixa é a mesma que havia sido recomendada pelo Ministério da Saúde para casos graves e a alta foi a que havia sido usada em pacientes chineses.
Inicialmente, o estudo previu a inclusão de 440 pacientes hospitalizados já em estado grave, no Hospital Delphina Aziz, referência para covid-19 no Amazonas. Os testes começaram no dia 23 de março. Com alguns dias de trabalho, foi registrada a morte de 11 pacientes dos dois grupos, mas notou-se mais efeitos colaterais no grupo com a dose alta e ela foi suspensa. Todos os pacientes começaram a usar a dose mais baixa a partir do dia 6 de abril, segundo explicou em nota o infectologista Marcus Lacerda, da Fiocruz, líder do estudo.
"A primeira conclusão foi que pacientes graves com covid-19 não deveriam mais usar a dose recomendada no consenso chinês, fato que até o momento não se tinha qualquer evidência, uma vez que nenhum estudo realizou adequadamente a avaliação de segurança, como eletrocardiogramas diários, como feito em Manaus, sob assessoria de cardiologistas experientes e renomados. Dose altas parecem ser seguras em pacientes com câncer, mas não em pacientes graves com covid-19, em especial os mais idosos. Uma possível explicação levantada no artigo é a ocorrência de miocardite, ou seja, inflamação do músculo cardíaco", escreveu Lacerda.
"O estudo não permite em absoluto concluir que a cloroquina em doses baixas funciona ou não para covid-19, porque não tem o grupo comparador de controle, ou seja, sem usar a medicação. Outros estudos para responder a essa questão, estão sendo realizados nesse momento, em outras partes do planeta", continuou.
Os pesquisadores comunicaram à Conep e o resultado veio à tona, justamente por ter trazido um primeiro resultado negativo para o uso da cloroquina. Uma reportagem grande sobre o assunto saiu no New York Times, chamando a atenção para os potenciais riscos com base nos resultados preliminares do trabalho e a pesquisa caiu nas redes sociais. Postagens indicavam que todas as mortes teriam ocorrido por causa do uso da dose mais alta. Uma mensagem inicial, que viralizou, dizia que o estudo era irresponsável e que os pesquisadores tinham usado os pacientes como "cobaias humanas".
"Algo absolutamente incorreto", disse Lacerda, "já que todos os requisitos éticos e legais foram rigorosamente seguidos". Ele explicou que todo o procedimento foi aprovado pelos comitês de ética e, dos 11 mortos, havia pessoas dos dois grupos: dose baixa e o de alta.
"A interpretação equivocada do ativista e seus seguidores foi de que todas as mortes ocorridas no estudo se deveram ao uso das altas doses, sendo que nem todos os pacientes usaram a alta dose e todos eles tinham covid-19 muito grave, vindo a falecer por conta da doença, o que ocorreu dentro da média mundial."
Lacerda relatou ainda que as reações escalaram para o nível de agressão. "Uma onda de reações de natureza ideológica, de pessoas que nunca leram o estudo na íntegra, sem qualquer formação científica, motivou manifestações violentas de cunho pessoal ao pesquisador principal, sua família e sua equipe, o que tem desviado a atenção e o foco do trabalho realizado aqui durante a pandemia", escreveu.
"Pacientes e seus familiares estão com medo do que pode ter acontecido na pesquisa, apesar da equipe estar em constante contato com todos os participantes e seus familiares, com o objetivo de orientar e confortar pessoas que já passaram por imenso trauma", disse. "O debate não apenas está tendo forte viés ideológico, mas também prejudicando a reputação de pesquisadores com forte tradição de pesquisa no Brasil e no mundo, o que pode ser um efeito deletério grave em momentos como o que estamos vivendo."