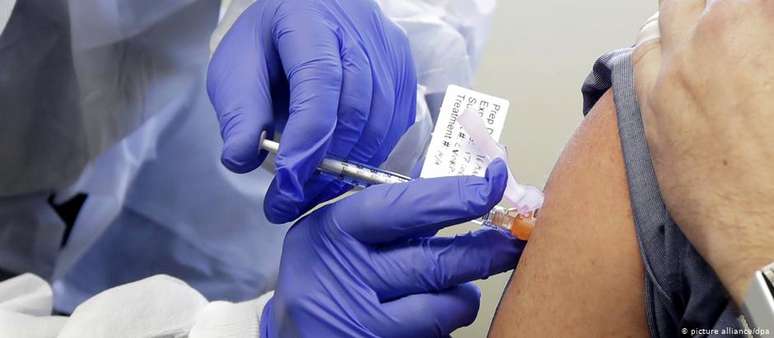
Como o Brasil se prepara para garantir a vacina à população
País está em posição relativamente segura na corrida pela imunização contra o coronavírus, avaliam especialistas
O Brasil teve uma reação lenta e descoordenada para frear a disseminação da covid-19, com o presidente Jair Bolsonaro e parte dos governadores questionando recomendações da comunidade científica sobre o tema. Como resultado, o país atingiu no último sábado 100 mil mortos pela doença e divide com Estados Unidos e Índia a liderança no número de novos casos diários. Os preparativos para a testagem, produção e distribuição de uma vacina eficaz, porém, colocam hoje o Brasil em uma situação relativamente segura na corrida para imunizar sua população, segundo especialistas consultados pela DW Brasil.
Há no mundo oito vacinas contra a covid-19 na fase 3 de ensaios clínicos, a última etapa antes da aprovação. Dessas, duas receberam apoio direto de autoridades brasileiras e já contam com acordos que envolvem a compra e produção em território nacional: a desenvolvida pela universidade britânica de Oxford em parceria com o laboratório AstraZeneca, escolhida pelo governo federal, e a criada pela chinesa Sinovac, que tem o governo de São Paulo como parceiro.
As duas adotam tecnologias distintas, com vantagens e desvantagens. A aposta do presidente Jair Bolsonaro foi a de Oxford, por meio de uma parceria com a Fundação Oswaldo Cruz, instituição pública sediada no Rio de Janeiro. Na quinta-feira passada, o presidente assinou uma medida provisória abrindo crédito de R$ 1,9 bilhão para adquirir a tecnologia e oferecer 100 milhões de doses para brasileiros até meados de 2021, sendo 30 milhões ainda neste ano se a vacina se mostrar eficaz, distribuídas pelo Sistema Único de Saúde (SUS).
Paralelamente, o governador de São Paulo, João Doria, aplica recursos paulistas em uma parceria entre o Instituto Butantan, órgão público de pesquisas biológicas, e a empresa chinesa Sinovac. Se apresentar bons resultados, poderiam ser produzidas no País 30 milhões de doses dessa vacina até janeiro de 2021.
A escolha do governo federal
A opção do Ministério da Saúde pela vacina da Oxford/AstraZeneca começou a ser costurada no final de junho, quando a Fiocruz assinou um acordo prévio de cooperação para transferência de tecnologia e recebimento de insumos. A parceria foi confirmada em 31 de julho e viabilizada financeiramente pela medida provisória da semana passada.
Marco Krieger, vice-presidente de Produção e Inovação em Saúde da Fiocruz, afirma à DW Brasil que o País fez um contrato de encomenda tecnológica, que permite a aquisição de uma tecnologia que ainda não está pronta, e inclui todos os passos para a sua nacionalização completa, que poderia ser alcançada no meio do ano que vem.
Até lá, a Fiocruz ainda dependeria da importação do princípio ativo da vacina, cuja compra também foi assegurada pela medida provisória e seria produzido pela AstraZeneca. Caberia à fundação brasileira então realizar os outros passos da produção, como formulação, envase, rotulagem e controle de qualidade.
Nessa transição, a Fiocruz poderia entregar 30 milhões de doses ainda neste ano e 70 milhões no primeiro semestre de 2021. "De forma paralela, estaremos fazendo a transferência total da tecnologia", com capacidade para realizar todos os passos da produção no país no segundo semestre, diz Krieger.
Ele estima que até outubro haverá dados preliminares sobre a fase 3 do ensaio clínico, que se forem positivos permitiriam a obtenção de um registro emergencial da vacina junto à Anvisa. Segundo ele, não haverá pagamento de royalties nem à Universidade de Oxford nem ao laboratório AstraZeneca, mas apenas a cobertura dos custos de produção adicionados a uma taxa de no máximo 20% para cobrir gastos com pessoal e manutenção de estrutura.
A Fiocruz teria capacidade para fabricar 40 milhões de doses por mês. Para ampliar suas instalações, a medida provisória destina parte das verbas para reformar uma fábrica da fundação e comprar equipamentos necessários para produzir o princípio ativo da vacina no país. Na semana passada, a Fiocruz também recebeu uma doação de R$ 100 milhões de empresas e fundações com o mesmo objetivo.
Além de ser apoiada por iniciativas internacionais para a imunização da população mundial contra a covid-19, como a GAVI Alliance, a vacina de Oxford chamou a atenção da Fiocruz por utilizar uma tecnologia que tem sinergia com um dos atuais focos da fundação, a produção de biofármacos - uma nova geração de medicamentos produzidos a partir da biossíntese em organismos vivos.
Ao contrário dos medicamentos sintéticos, que são moléculas pequenas produzidas quimicamente, os biofármacos são proteínas úteis para tratar e curar doenças. Essas proteínas são produzidas por células vivas hospedeiras, em equipamentos conhecidos como biorreatores. Esse processo é realizado pelo Instituto de Tecnologia em Imunobiológicos (Bio-Manguinhos) da Fiocruz.
A vacina de Oxford funciona dessa forma. Após obter o código genético da proteína spike presente no coronavírus, usada para penetrar nas células humanas, os cientistas modificaram um outro vírus, que causa infecções em chimpanzés mas não em humanos, para que ele produza essa proteína e provoque uma reação imunológica da pessoa que recebeu a vacina, tornando-a protegida caso venha a ter contato com o coronavírus. Trata-se de uma tecnologia nova e promissora, mas que ainda não se mostrou efetiva em nenhuma vacina aplicada em humanos.
"Levamos em consideração a tecnologia que poderia ser mais rapidamente interiorizada na Fiocruz. É algo que a gente já usa em outros produtos", diz Krieger. Ele afirma que, se a vacina de Oxford não mostrar bons resultados, ou após a população já ter sido imunizada, a estrutura adquirida pela fundação poderá ser usada para produzir outros medicamentos e vacinas com a mesma tecnologia.
Ele está otimista em relação às chances de sucesso da vacina em teste no Brasil. "Com apenas uma dose ela já mostrou alto nível de voluntários que produziram anticorpos, mais de 91%, e quem tomou duas doses, 100%. Há chance gigantesca que essa vacina possa ser utilizada", diz.
A aposta paulista
Em 11 de junho, duas semanas antes do acordo inicial firmado entre a Fiocruz e Oxford/AstraZeneca, o Instituto Butantan e a Sinovac assinavam um termo para testar a vacina chinesa em 9 mil brasileiros, em um processo bancado por R$ 85 milhões do governo paulista.
O Butantan e a empresa chinesa já estavam em contato há algum tempo. Em agosto de 2019, uma missão composta por Doria e dirigentes de órgãos do governo paulista foram à China para inaugurar um escritório comercial de São Paulo em Xangai, e aproveitaram para visitar alguns produtores de vacina, incluindo a Sinovac. Após o início da pandemia, houve nova aproximação.
"A Sinovac, entre nossos parceiros, já tinha vacina em condições de ir para o estudo clínico e fizemos a associação. É um acordo de interesse mútuo. A Sinovac precisando fazer seu estudo clínico, e o Butantan precisando ter uma vacina em condições de avançar rapidamente", afirma à DW Brasil Dimas Tadeu Covas, diretor do Instituto Butantan.
Ele estima que, até o final de setembro, todos os voluntários já terão recebido a vacina, e que a avaliação de sua eficácia ocorra até o final do ano. Segundo Covas, o acordo com a Sinovac permite que o Butantan comece a envasar a vacina em outubro, com capacidade de entregar 30 milhões de doses em janeiro de 2021. O princípio ativo viria da China, e caberia ao Butantan completar a fórmula, distribuí-la em frascos, fazer a rotulagem e o controle de qualidade.
Paralelamente, o Butantan já está adaptando uma de suas fábricas, em São Paulo, cuja reforma deve terminar em maio de 2021, para produzir a vacina integralmente em território nacional. "A partir daí, poderíamos ter todo o processo aqui, desde o cultivo [do vírus]", diz Covas. Ainda não há acordo sobre a transferência de tecnologia, mas ele afirma que o Butantan se tornou "sócio dessa vacina" ao investir recursos próprios na fase 3 de ensaio clínico.
A tecnologia usada pela Sinovac é tradicional na área. Trata-se do próprio vírus que causa a covid-19, mas inativado. Ele é incapaz de provocar uma infecção, mas provoca na pessoa inoculada uma reação imunológica que a protege caso venha a ter contato com o coronavírus vivo.
Covas afirma que ainda não há estimativa de custos para produzir a vacina no Brasil, mas que deverá ser baixo comparado às outras vacinas em teste. Assim como Krieger, da Fiocruz, ele se mostra otimista. "Pode não ter o nível de eficácia desejado, pode ter 90%, 95%, mas em uma pandemia, dependendo do nível, essa vacina só não será utilizada se não tiver nenhum efeito. Mas não acredito nisso."
Para o diretor do Butantan, a vacina da Sinovac "é a mais próxima de chegar à população no Brasil", por usar uma tecnologia tradicional, já dominada pelo Butantan. "As outras vacinas são absolutamente novas, ainda não comprovadas do ponto de vista da tradição e da produtividade", diz.
Covas afirma que o instituto não foi procurado em nenhum momento pelo Ministério da Saúde antes da decisão do governo federal de apostar na vacina da Oxford/AstraZeneca.
"Preliminarmente, não houve nenhuma conversa, nenhuma interrogação, nenhuma pergunta. Ontem [quinta-feira, 06/08], o secretário de Vigilância e Saúde [do Ministério da Saúde] disse que o ministério adquirirá a vacina que ficar pronta em primeiro lugar, e está disposto a vir aqui conhecer a vacina no Butantan, e marcou data", conta, ressalvando que acharia "ótimo" se tanto a vacina de Oxford/AstraZeneca quanto à da Sinovac dessem bons resultados.
A posição do Brasil na fila
O fato de o Brasil ter potenciais vacinas sendo testadas em sua população, com acordos encaminhados que permitiriam a aquisição e a produção interna, é considerado positivo, segundo o virologista Flávio Fonseca, pesquisador do Centro de Tecnologia de Vacinas da Universidade Federal de Minas Gerais (UFMG).
"Estava muito preocupado com a posição que o Brasil ficaria na fila que irá se formar quando as primeiras vacinas derem certo. Não havia nenhum movimento do governo federal para colocar o País numa posição mais favorável. Mas houve esse movimento tardio do governo, que achei válido e adequado", afirma.
Ele diz que a vacina de Oxford/AstraZeneca, por usar uma tecnologia nova, tem um maior grau de incerteza. Mas, caso mostre bons resultados, deverá alcançar uma eficácia maior com apenas uma dose por pessoa e tem um processo de fabricação que exige requisitos de segurança mais baixos.
Já a tecnologia da Sinovac, diz, é "clássica", usada por exemplo na vacina para a gripe distribuída no Brasil. Em contrapartida, por envolver a manipulação do próprio vírus, sua fabricação demanda um maior nível de biossegurança. Além disso, caso funcione, deve exigir a aplicação de duas ou três doses.
"Toda vacina que inclui um vírus vivo, como é a da AstraZeneca, estimula mais o sistema imune da pessoa vacinada. Já as com o vírus morto [como a da Sinovac] estimulam menos, e necessariamente será usada mais de uma dose", afirma.
Fonseca alerta que ainda não é certo que uma das duas vacinas apresentará bons resultados e que os brasileiros não devem criar "uma expectativa ou euforia falsa". Mas que pelo menos duas das vacinas sendo hoje testadas no mundo devem apresentar boa eficácia.
Uma vez desenvolvida a vacina e superada a fase de produção, ele crê que o país estará bem posicionado para a sua distribuição. "O Brasil tem um dos melhores programas de vacinação pública do mundo e a expertise para entregar a vacina para o País inteiro. Claro que isso será levado a um limite não testado", diz.
Ele prevê que, inicialmente, serão vacinadas as pessoas na linha de frente do sistema de saúde, como médicos e enfermeiros, profissionais de categorias que não podem parar, como motoristas de ônibus e policiais, e pacientes mais suscetíveis ao agravamento da covid-19, como idosos e portadores de comorbidades.