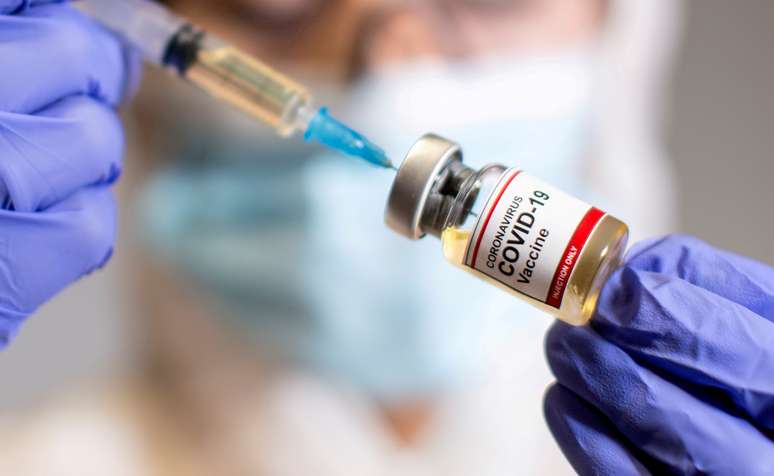
Anvisa terá 5 dias para analisar vacina autorizada fora
A Câmara dos Deputados aprovou MP prevê que toda vacina aprovada pela Anvisa será adquirida e distribuída para a população
A Câmara dos Deputados aprovou, nesta sexta-feira, medida provisória que prevê a inclusão de todas as vacinas contra Covid-19 aprovadas pela Agência Nacional de Vigilância Sanitária (Anvisa) no plano nacional de imunização e estabelece prazo de cinco dias para a agência autorizar um imunizante que já tenha sido aprovado por autoridades sanitárias internacionais.
Originalmente destinada a formalizar a adesão do Brasil ao consórcio Covax Facilities, que prevê a distribuição de vacinas de forma igualitária no mundo, a MP foi alterada na Câmara para incluir recomendações ao plano de vacinação.
Se aprovada pelo Congresso e sancionada, a proposta transformará em lei o que foi prometido pelo Ministério da Saúde ao apresentar esta semana o plano de vacinação, que toda vacina aprovada pela Anvisa será adquirida e distribuída para a população.
Além disso, o texto estabelece que a Anvisa terá cinco dias a partir do pedido para aprovar uma vacina que tenha sido aprovada por ao menos uma de oito autoridades sanitárias internacionais. Foram listas as agências dos Estados Unidos, União Europeia, Japão, China, Canadá, Reino Unido, Coreia do Sul, Argentina e Rússia.
"As condições de registro e de autorização de uso deverão ser as mesmas do país de origem, e o fabricante deve se comprometer a concluir estudos clínicos em curso. A compra de vacinas poderá ser feita pela União ou por Estados e municípios", informou a Agência Câmara Notícias.
Países como Estados Unidos e Reino Unido já iniciaram suas campanhas de vacinação contra a Covid-19, após suas agências reguladoras terem aprovado o uso emergencial da vacina desenvolvida pela Pfizer. No Brasil, a previsão do governo é iniciar a vacinação em janeiro.
Uma lei aprovada pelo Congresso este ano já estabelece prazo de 72 horas para que a Anvisa avalie a importação e distribuição de medicamentos e insumos para combate à Covid-19 registrados em EUA, UE, Japão e China, mas a agência afirma que essa legislação não se aplica aos casos de uso emergencial de vacinas.
A proposta aprovada agora pela Câmara determina preferência a imunizante que seja produzido no Brasil, ou por empresa brasileira sediada no exterior, ou ainda produzido por empresas que invistam em pesquisa e no desenvolvimento de tecnologia no Brasil.
"O Poder Executivo federal, por intermédio do Ministério da Saúde, deverá adquirir e distribuir aos Estados, ao Distrito Federal e aos Municípios vacinas contra o Covid-19 registradas na Agência Nacional de Vigilância Sanitária (Anvisa) ou que tenha autorização excepcional e temporária para a importação e distribuição, na forma da lei", diz artigo do texto.
O texto de Zuliani aprovado pelos deputados não incluiu a polêmica previsão de um termo de consentimento a ser assinado pelas pessoas que receberem doses das vacinas autorizadas em caráter emergencial pela Anvisa.
A inclusão do termo havia sido pedida pessoalmente pelo presidente Jair Bolsonaro, mas, na terça-feira, o presidente da Câmara, Rodrigo Maia (DEM-RJ), anunciou que a controversa previsão não entraria no texto.
Um destaque aprovado pela Casa inseriu no texto determinação para que, no caso das vacinas autorizadas, seja dispensada a assinatura de quaisquer termos de responsabilidade ou de consentimento por parte das pessoas, mesmo se a regra constar de outras normas.
Especialistas afirmam que a obrigatoriedade de assinatura de um termo de consentimento pode desencorajar a vacinação, prejudicando os esforços para conter uma epidemia que já deixou quase 183 mil mortos no Brasil.