Área técnica recomenda aprovação de vacina da Janssen
Cinco diretores da Anvisa irão votar e decidir sobre uso emergencial no imunizante contra a covid-19 no Brasil
A Gerência Geral de Medicamentos da Agência Nacional de Vigilância Sanitária (Anvisa) recomendou nesta quarta-feira a aprovação do pedido de uso emergencial no Brasil da vacina contra covid-19 da Janssen, uma subsidiária da Johnson & Johnson.
O órgão regulador decide nesta quarta, em reunião extraordinária, sobre o pedido feito pela Janssen para o uso emergencial da vacina do laboratório no Brasil. Após a recomendação da área técnica, os cinco diretores da Anvisa irão votar sobre o pedido.
A área técnica da agência pontuou algumas incertezas, no entanto, sobre o imunizante, como os diferentes locais de fabricação em larga escala e a falta de evidências sobre a eficácia da vacina contra novas variantes do coronavírus.
"Os dados apresentados até o momento dão suporte ao uso emergencial da vacina e não se vislumbra um risco à saúde da população relacionado aos dados faltantes no momento que seja superior à não utilização da vacina", disse a Gerência Geral de Medicamentos em apresentação sobre a vacina.
O Brasil possui acordo com a Janssen para a aquisição de 38 milhões de doses da vacina da empresa, com previsão de entrega de 16,9 milhões de doses entre julho e setembro e 21,1 milhões de outubro a dezembro.
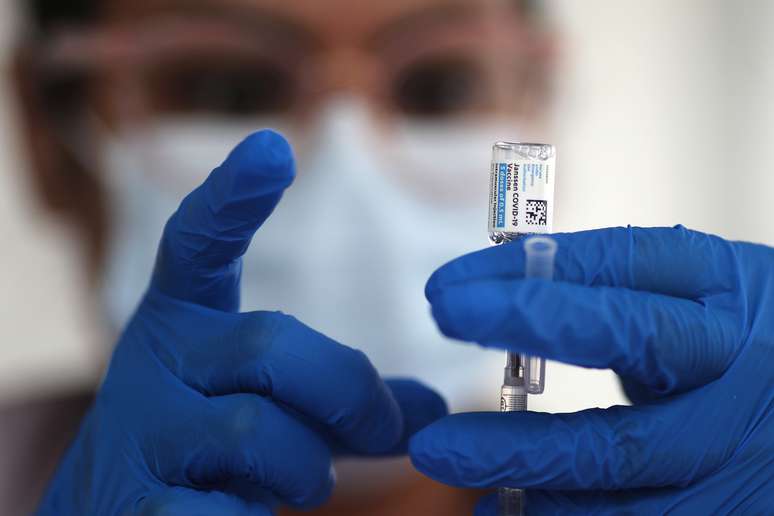
A vacina do laboratório da Johnson & Johnson se destaca por requerer somente o uso de uma dose. O imunizante já tem sido utilizada nos Estados Unidos.



-1hrdo12wsdoaa.jpg)

-t4kmlaxgwhma.jfif)