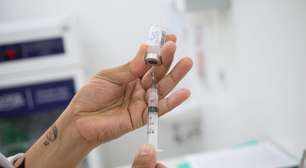
Brexit pode ter ajudado o Reino Unido a liberar vacina
Diretor diz que a decisão da agência reguladora britânica de avaliar a vacina abriu precedente para colocar o país 'na frente da fila'
O Brexit pode ter ajudado o Reino Unido a vencer a corrida por uma vacina da covid-19, disse o líder de uma grande empresa farmacêutica em meio a críticas internacionais sobre a velocidade de aprovação da vacina pelo país, noticiou nesta quinta-feira, 3, o jornal britânico Daily Telegraph.
Hugo Fry, o diretor-gerente da Sanofi no Reino Unido, uma multinacional sediada em Paris e a quinta maior fabricante de medicamentos do mundo, disse ao jornal que a "desassociação dos mecanismos regulatórios e de compra da UE permitiu a compra ágil" de centenas de milhões de doses e uma rápida luz verde para a aprovação à vacina da Pfizer / BioNTech.
Fry disse que a decisão da Agência Reguladora de Medicamentos e Produtos de Saúde (MHRA) de avaliar a vacina em caráter de emergência - condensando o trabalho de muitos meses em algumas semanas - abriu um precedente que pode colocar o Reino Unido na "frente da fila" para medicamentos futuros.
A resposta veio após a Agência Europeia de Medicamentos (EMA), que atua em nome dos 27 Estados-membros da UE, sugeriu que o Reino Unido "sacrificou o rigor no interesse da velocidade" - uma sugestão que a MHRA negou firmemente.
Enquanto isso, um ministro da saúde alemão disse que os países da UE decidiram não buscar a aprovação emergencial para "manter a solidariedade do bloco".
Fry, que se opôs ao Brexit, disse que a decisão do MHRA de avaliar o medicamento independentemente da EMA e por meio de um método de "revisão contínua" - análise de provas assim que elas chegaram - foi crucial para a aprovação rápida.
"É um bom exemplo do que eles podem fazer quando se empenham nisso", disse ele em entrevista ao The Telegraph. "Não há dúvida de que o Reino Unido tem uma das agências reguladoras de medicamentos mais respeitadas e melhores do mundo".
"Isso mostra que se você se sentar com o MHRA e discutir o caminho e um possível acordo rápido em andamento, ele pode trazer medicamentos inovadores realmente bons muito rapidamente para os pacientes do Reino Unido."
A própria Sanofi, um dos principais fornecedores da vacina contra a gripe, está desenvolvendo uma vacina contra a covid, que espera-se que entre em produção a partir de junho.
Fry elogiou a flexibilidade do Grupo de Trabalho de Vacinas do Reino Unido, que até agora garantiu acesso a 357 milhões de doses de vacinas de sete fabricantes diferentes. O Reino Unido foi o primeiro país do mundo a pré-encomendar suprimentos da vacina da Pfizer, garantindo 40 milhões de doses.
"Eles têm sido rápidos e têm uma seleção realmente boa e bons volumes", disse Fry. "Não estou convencido de que, se eles tivessem participado desse programa de compras europeu, teriam tido bastante velocidade e flexibilidade para fazê-lo."
Falando sobre sua própria negociação com o governo, ele disse: "o fato de o Reino Unido ter sido capaz de fazer isso em um único acordo significa que ele conseguiu a vacina antes da França e da Alemanha. Ou seja: é mais eficiente."
Os comentários surgiram quando a Agência Europeia de Medicamentos sugeriu que o motivo pelo qual o procedimento de regulamentação da europa demorou mais era porque "requeria mais provas".
"A EMA considera que a autorização de comercialização condicional [em oposição à autorização de emergência] é o mecanismo regulador mais apropriado para uso na atual emergência pandêmica, para conceder a todos os cidadãos da UE acesso a uma vacina e para apoiar campanhas de vacinação em massa", disse um porta-voz.
Guido Rasi, um ex-chefe da agência, disse: "Pessoalmente, eu esperava uma revisão robusta de todos os dados disponíveis, o que o governo britânico não fez apenas para poder dizer que sem a Europa você está em primeiro lugar."
Vários políticos europeus criticaram a insistência do Governo do Reino Unido de que, nas palavras de Alok Sharma, o Secretário de Negócios, "vamos lembrar este momento como o dia em que o Reino Unido liderou o ataque da humanidade contra esta doença".
O ministro da saúde alemão, Jens Spahn, disse após uma reunião de ministros da saúde da UE: "A ideia não é que sejamos os primeiros, mas a ideia é ter vacinas seguras e eficazes na pandemia. Preferimos ter um procedimento regulatório condicional, usando um procedimento experimentado e testado. Isso pode levar a alguma diferença no tempo. "
Andreas Michaelis, o embaixador alemão no Reino Unido, disse: "Por que é tão difícil reconhecer este importante passo a frente como um grande esforço e sucesso internacional? Eu realmente não acho que esta seja uma história nacional. Apesar da empresa BioNTech sendo uma empresa alemã, uma contribuição crucial, ela é europeia e transatlântica. "
Falando em Downing Street na noite de quarta-feira, Boris Johnson se recusou a ser tentado a declarar a aprovação do MHRA como evidência da superioridade britânica, em vez disso, disse que o avanço foi a conquista de "muitas pessoas".
No entanto, Matt Hancock, o Secretário de Saúde, identificou explicitamente o Brexit como uma razão para a rápida aprovação do Reino Unido.
"Até o início deste ano, estávamos na Agência Europeia de Medicamentos. Por causa do Brexit, pudemos tomar a decisão de fazer isso com base no regulador do Reino Unido, um regulador de classe mundial, e não ir no ritmo dos europeus, que estão se movendo um pouco mais devagar ", disse ele.








-1hbdpb3fwc01l.jpg)

-sokmk4mgqnuf.jpg)
-vb42vq99hf8h.png)