Fiocruz pede uso emergencial da vacina de Oxford à Anvisa
Imunizante desenvolvida pela AstraZeneca já é aplicado no Reino Unido
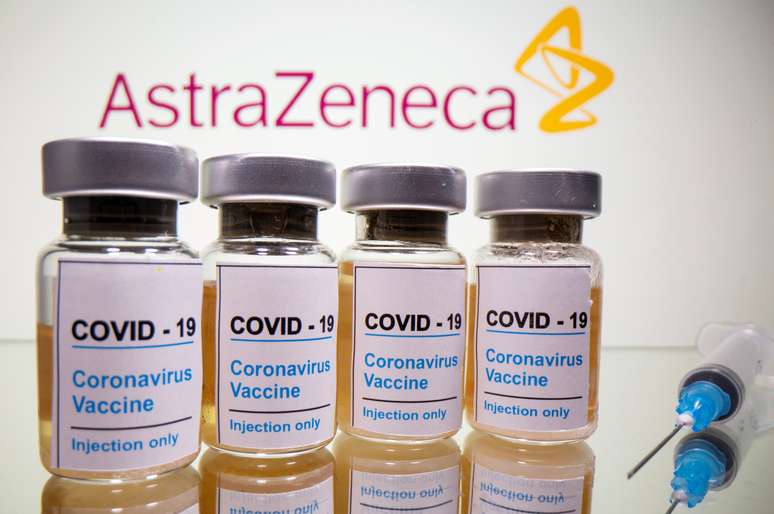
A Fundação Oswaldo Cruz (Fiocruz) pediu à Agência Nacional de Vigilância Sanitária (Anvisa) autorização para uso emergencial da vacina contra a covid-19 desenvolvida pela AstraZeneca e pela Universidade de Oxford.
"O pedido da Fiocruz é para o uso de 2 milhões de doses de vacinas que devem ser importadas do laboratório Serum, sediado na Índia. O laboratório é um dos fabricantes da vacina da AstraZeneca", disse a Anvisa em nota.
O órgão regulador já havia autorizado a importação das doses, que poderão ser usadas para iniciar a imunização nos brasileiros enquanto a Fiocruz inicia a produção no país da mesma vacina.
O imunizante é a principal aposta do governo federal para a vacinação dos brasileiros a fim de conter a pandemia do novo coronavírus no país. Até o fim do ano, o governo federal espera contar com 210 milhões de doses da vacina da Fiocruz.
Esperava-se que a Fiocruz apresentasse a solicitação até quarta-feira, mas pedidos adicionais de informações por parte da Anvisa a respeito da vacina a ser importada da Índia adiaram essa data para esta sexta-feira.
Como o prazo da Anvisa para avaliar uso emergencial de vacinas é de até dez dias, a expectativa é que a autorização para esse tipo de aplicação pela Fiocruz saia até 18 de janeiro. Entre três possibilidades de datas do Ministério da Saúde para iniciar a imunização nacional contra o novo coronavírus, a mais otimista veria a partida dada em 20 de janeiro.
Nesta sexta-feira, a Anvisa também recebeu o pedido do Instituto Butantão para autorização temporária de uso emergencial e em caráter experimental da Coronavac.
Sem detalhar os dados, o Butantã afirma que a Coronavac tem eficácia de 78% para evitar casos leves do novo coronavírus e de 100% par quadros moderados e graves. O Ministério da Saúde pretende comprar 100 milhões de doses da vacina em 2021, ou seja, toda a produção do instituto.
* Com informações do Estadão Conteúdo e Reuters