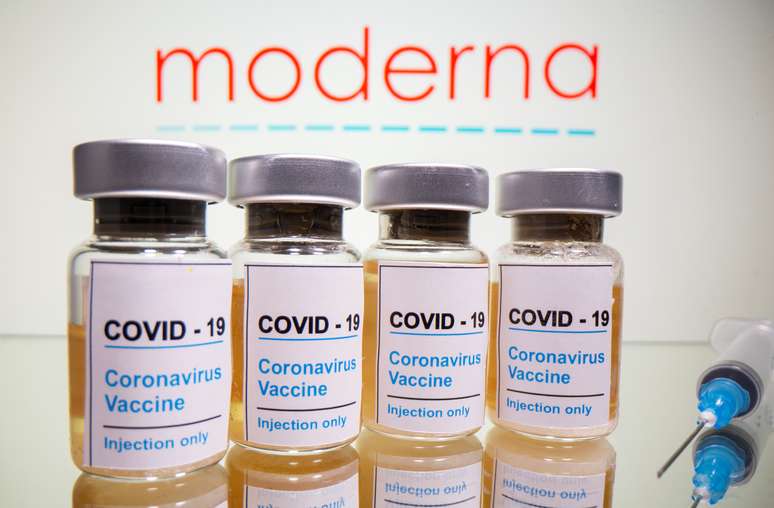
Moderna buscará autorização emergencial nos EUA e na UE
Estudos em estágio avançado que mostraram que a vacina tem eficácia de 94,1% sem preocupações graves de segurança
A Moderna anunciou nesta segunda-feira que pedirá autorização para uso emergencial de sua potencial vacina contra covid-19 nos Estados Unidos e na Europa com base em resultados completos de estudos em estágio avançado que mostraram que a vacina tem eficácia de 94,1% sem preocupações graves de segurança.
A empresa também relatou que o imunizante teve 100% de sucesso na prevenção de casos graves da doença. A informação coloca a Moderna como a segunda empresa que deve receber autorização para uso emergencial de sua vacina nos EUA ainda neste ano.
"Acreditamos que temos uma vacina que é altamente eficaz. Agora temos os dados para provar isso", disse o chefe médico da Moderna, Tal Zaks, em entrevista por telefone. "Esperamos desempenhar um papel importante na virada sobre esta pandemia."
Zaks disse ter ficado emocionado ao ver o resultado de eficácia de 94,1% no fim de semana: "Foi a primeira vez que eu me permiti chorar. Neste nível de eficácia, quando você faz as contas do que significa para a pandemia que está nos devastando, é esmagador".
O anúncio da Moderna vem depois de notícias da Pfizer e de sua parceria alemã BioNTech de que a candidata a vacina de ambas tem 95% de eficácia. A Pfizer pediu autorização para uso emergencial nos EUA e está cerca de uma semana à frente da Moderna.
Além do pedido nos EUA, a Moderna disse que também solicitará aprovação condicional na Agência Europeia de Medicamentos, que já iniciou uma análise contínua dos dados.